Критерії оцінювання навчальних досягнень з хімії
Вивчити і здати на уроці обов'язково усім, хто не здав!!!
===============================================
Дата: 21/05 ( 9А, 9Б)
Тема: Повторення: хімічні реакції , розрахункові задачі за рівняннями реакцій.
Цілі уроку:
- повторити окисно-відновні реакції, їх класифікацію;
- закріпити уміння розвязувати задачі за рівнянням реакції
===============================================
Дата: 16/05 ( 9А, 9Б)
Тема: Повторення: хімічні реакції , розрахункові задачі на приготування розчинів
Цілі уроку:
- повторити розрахункові задачі за участі розчинів;
- закріпити уміння складати алгоритм задачі за особливостями її умови (приготування розчинів, змішування розчинів, реакції з розчинами речовин);
1)Повторіть розрахункові формула за участі розчинів.
2) Опрацюйте питання
1. Що таке кількісна характеристика розчину? (Масова частка розчиненої речовини або концентрація розчину).
2. За якою формулою обчислюється масова частка?
3. Як обчислити масу розчиненої речовини, користуючись цією формулою?
4. Як обчислити масу розчинника?
3) Пригадайте алгоритм розвязування задач на змішування розчинів за прикладом.
Задача Які маси розчиненої речовини та води містяться в розчині масою 320г з масовою часткою розчиненої речовини 40%? Як зміниться масова частка речовини, якщо до розчину долити 80мл води?
![]() Дано: Розв`язання
Дано: Розв`язання
![]() m(роз-ну) = 320г Формули для обчислення:
m(роз-ну) = 320г Формули для обчислення:
![]()
![]() w(речов.)=40%
w(речов.)=40% 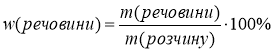 ;
;
![]()
![]()
![]()
![]() V2(H2O)=80мл
V2(H2O)=80мл ![]()
m (H2O)-? 1)m (речовини)=![]()
m(речов.)-? 2) m(H2O)=m(розч)-m(речовини)=320г – 128г =192г
w2(речов.)=? 3) При додаванні води змінилася лише маса розчину, маса речовини залишилася такою ж як була:
m2(розчину)= m(розчину)+ m2(H2O)=320г + 80г=400г
m2(речовини)= m(речовини.)=128г
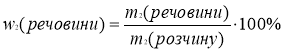
w2(речов.)= ![]() =32%
=32%
Відповідь: m(речовини) = 128г; m(H2O)=192г; w2(речовини)=32%.
4) Перегляньте відеоурок про задачі, з використанням рівнянь реакцій
Задачі з рівняннями реакцій з розчинами
5) Виконайте самостійно задачу.
Обчисліть масу розчину етанолу з масовою часткою спирту 92 %, який можна приготувати зі спирту, отриманого при бродінні глюкози масою 720г
===============================================
Дата: 14/05 ( 9А, 9Б)
Тема: Повторення: розчини , електролітична дисоціація.
Цілі уроку:
- повторити класифікацію розчинів. поняттяелектролітів та електролітичної дисоціації;
- закріпити уміння складати рівняння реакцій за участі електролітів;
1)Повторити матеріал підручника §6, 7, 10
2) Перегляньте відеоурок з теми
3) Повторіть алгоритм складання йонних рівнянь
4) виконайте самостійно завдання в останньому відеоролику
===============================================
Дата: 09/05 ( 9А, 9Б)
Тема: Хімічна наука і виробництво в Україні . Видатні вітчизняні вчені -- творці хімічної науки.
Цілі уроку:
- переконатися у важливості розвитку хімічної науки;
- отримати відомості про вчених хіміків — лауреатів Нобелівської премії;
- дізнатися про розвиток хімії в Україні й підготовку майбутніх хіміків.
1) Опрацюйте матеріал підручника §38
2) Перегляньте відеоурок з теми
3) Опрацюйте презентацію
4) Приготуйте коротеньке повідомлення про лауреатів Нобелівської премії в області хімії
Дата: 30/04 ( 9А, 9Б) - 02/05 (9-А, 9-Б)
Тема: Місце хімії серед наук про природу, її значення для розуміння наукової картини світу. Значення хімії у розвитку цивілізації
Цілі уроку:
- ознайомитися із взаємозв'язками природничих ;
- визначити значення хімії у розвитку наукового сприйняття світу
- розширити свої знання про розвиток хімічної науки та її значення для людства
1) Опрацюйте матеріал підручника §37
2) Перегляньте відеоурок з теми
Місце хімії серед природничих наук
3) Поміркуйте над питаннями:
- Чому штучним матеріалам часто надають перевагу порівняно з матеріалами природного походження?
- Які хімічні волокна використовують при виробництві тканин?
- Назвіть переваги і недоліки побутового посуду із пластмаси.
- Які знання з хімії вам знадобилися в житті?
- Запропонуйте спосіб очищення відпрацьованого промислового
газу (основні компоненти — азот, кисень, водяна пара) від доміш
ки сірководню
4) Письмово у зошиті виконайте завдання ( прикріпити на 30/04)
За матеріалами з інтернету з’ясуйте, які речовини використовують у медицині для заміни пошкоджених або зламаних кісток.
5) Домашнє завдання на 02/05
Приготувати презентацію (або розповідь, колаж) на тему
"Значення хімії та хімічних знань у моєму повскденному житті"
- вказати які речовини, виготовлені за допомогою хімічного виробництва ти використовуєш;
- які знання з курсу хімії розширили твоє розуміння про користь або шкоду тих чи інших речовин, що використовуються у побуті.
- які висновки ти зробив про значення вивчення хімії на уроках (тільки чесно, без пафоса)
===============================================
Дата: 23/04 ( 9А, 9Б)
Тема: Білки як біологічні полімери, їх утворення, властивості, значення.
Цілі уроку:
- ознайомитися з будовою та властивостями білків;
- вивчити функції білків;
- розширити свої знання про значення білків для живих організмів.
1) Опрацюйте матеріал підручника §33
2) Перегляньте відеоурок з теми
3) Зверніть увагу на якісні реакції на білки
а) біуретова - доводить наявність пептидних зв'язків
б) ксантопротеїнова - доводить наявність ароматичних радикалів
4) Усно дайте відповіді на питання
- Які сполуки називають білками?
- Які функції вони виконують у живих організмах?
- Охарактеризуйте якісний склад білків.
- Як поводяться білки при нагріванні, додаванні розчинів деяких неорганічних сполук?
- Чому білкову їжу не можна замінити їжею, в якій переважають жири або вуглеводи?
===============================================
Дата: 18/04 ( 9А, 9Б)
Тема: Поняття про амінокислоти.
Цілі уроку:
- ознайомитися з будовою та властивостями амінокислот;
- вивчити функціональні групи амінокислот;
- розширити свої знання про значення амінокислот
1) Опрацюйте матеріал
Амінокислоти, їх склад. Амінокислоти — це органічні речовини, які можна назвати «цеглинками» білків. Вони широко розповсюджені в природі, оскільки входять до складу рослинних і тваринних організмів та організму людини.
Розглянемо склад молекул амінокислот.
Ви вивчили склад і будову молекули етанової кислоти (див. § 27). Як органічна кислота, вона містить у складі молекули властиву для всіх кислот карбоксильну групу -СООН, яка сполучена з групою атомів -СН3, що має назву радикал метил. Якщо в складі радикала молекули етанової кислоти СН3-СООН один атом Гідрогену замістити на аміногрупу -NH2, то утворюється амінокислота. Наприклад, H2N-CH2-COOH — аміноетанова кислота. Назва її походить від назви етанової кислоти з додаванням слова «аміно». Ця кислота найпростіша й містить по одній амінній і карбоксильній групі (рис. 119).

Рис. 119. Масштабна модель молекули аміноетанової кислоти
Якщо у складі радикала пропанової кислоти Н3С-СН2-СООН атом Гідрогену замінити на амінну групу, то отримаємо амінопропанову кислоту складу H2N-CH2-CH2-COOH і т. д.
Однак аміногрупа може розміщуватися не тільки на кінці молекули, а й біля іншого атома Карбону. Наприклад, біля атома Карбону, що безпосередньо з'єднаний з карбоксильною групою. Тоді склад молекули відображатиме формула:

Ця амінокислота має назву 2-амінопропанова, або α-амінопропанова. Саме такі амінокислоти входять до складу білків.
Дослідження молекул амінокислот показало, що до їх складу може входити не тільки по одній групі, як у складі найпростіших з них, а й більше. Є амінокислоти, молекули яких містять дві карбоксильні або дві аміногрупи.
Карбоксильні й аміногрупи проявляють різні хімічні властивості: перша — кислотні, друга — основні. В амінокислотах наявні й інші групи, зокрема гідроксильна -ОН, сульфідна -SH. Усі вони беруть участь в утворенні зв'язків. Саме завдяки цій унікальній властивості амінокислот структура білкової молекули дуже складна.
Фізичні властивості. Амінокислоти — кристалічні безбарвні речовини. Більшість з них добре розчинні у воді, мають високі температури плавлення. Серед великого розмаїття кислот у природі у складі білків, що містяться в організмі людини, є 20 α-амінокислот.
Про те, що основним структурним компонентом білків є амінокислоти, уперше заявив І. Горбачевський, виділивши їх у чистому вигляді.

Іван Якович Горбачевський (1854-1942) — український учений, хімік і біохімік, доктор медицини, уродженець Тернопільщини.
Працював професором кафедри лікарської хімії Карлового університету в Празі, ректором Українського вільного університету в Празі.
Уперше синтезував сечову кислоту з гліцину (аміноетанової кислоти) і вивчив утворення її в організмі. Виділив амінокислоти з білкових молекул тварин. Висловив думку про те, що білок складається з амінокислот.
Один із фундаторів української хімічної термінології, автор багатьох праць, підручників з неорганічної й органічної хімії українською мовою.
У 1902 р. Е. Г. Фішер сформулював пептидну гіпотезу про наявність у складі білків залишків молекул амінокислот.

Еміль Герман Фішер (1852-1919) — німецький хімік, член Берлінської академії наук, лауреат Нобелівської премії з хімії (1902). Професор хімії Мюнхенського, Ерлангенського, Вюрцбурзького університетів. У 1892 р. перейшов до Берлінського університету й працював там до кінця життя.
Написав наукові праці, присвячені синтезу органічних сполук. Синтезував глюкозу та фруктозу, уперше добув дипептид і підтвердив власну гіпотезу про наявність у складі білків залишків молекул амінокислот. Учений створив велику наукову школу. Його учнями були О. Дільс, А. Віндаус, Ф. Прегль, О. Варбург.
Речовини, що містять пептидний зв'язок, називають пептидами.
Унаслідок взаємодії молекул амінокислот утворюються дипептиди, трипептиди, поліпептиди. Побічним продуктом реакції є вода. Наприклад:

2) Перегляньте відеоурок
3) Дайте відповіді на питання:
- які характеристичні групи містять амінокислоти?
- чому амінокислоти вважають амфотерними сполуками?
- яке значення амінокислот для живих організмів?
4) Виконайте №242 з підручника.
===============================================
Дата: 11/04 ( 9А, 9Б)
Тема: Узагальнення та систематизація знань про оксигеновмісні органічні сполуки.
Цілі уроку:
- систематизувати знання про будову та властивості метанолу, етанолу, гліцерину, карбонових кислот , жирів та вуглеводів;
- повторити реакції хімічних властивостей етанолу, гліцерину, етанової кислоти, глюкози та інших вуглеводів;
- закріпити знання про взаємозвязки між класами оксигеновмісних неорганічних сполук.
1) Повторіть матеріал підручника §26- §32.
2) Пригадайте молекулярні та структурні формули
- спиртів метанолу, етанолу, гліцерину;
- етанової, стеаринової, пальмітинової, олеїнової, ленолевої та леноленової кислот;
- жирів;
- вуглеводів глюкози, фруктози, сахарози, крохмалю та целюлози.
3) Повторіть рівняння реакцій з етанолом, етановою кислотою, жирами та вуглеводами у конспекті.
4) Пригадайте алгоритм задач на визначення формули органічної речовини за відносною густиною , перегляньте відео Визначення формули
- Знаходимо молярну масу органічнох речовини М(реч) = Dгаз*М(газу)
- Записуємо загальну формулу речовини - спирт СnН2n+2О ; кислота СnН2nО2
- Складаємо математичне рівняння і знаходими n
- Записуємо формулу речовини , даємо їй назву.
5) Самостійно розв'яжіть задачу.
Визначте молекулярну формулу насиченого одноатомного спитру, якщо відносна густи його парів за киснем складає
===============================================
Дата: 09/04 ( 9А, 9Б)
Тема: Практична робота № 5. Виявлення органічних сполук у харчових продуктах.
Цілі уроку:
- повторити якісні реакції на етанол. гліцерин, етанову кислоту, глюкозу та крохмаль;
- навчитися виявляти означені речовин у продуктах харчування та застосовувати у практичному використанні.
1) Повторіть якісні реакції на етанол, гліцерин, етанову кислоту, глюкозу, крохмаль та ненасичені жири у робочому зошиті та правила ТБ при виконанні хімічних експериментів.
2) Виконайте роботу на платформі Мій Клас.
У кожному завданні є окремий відеоролик демонстрації якісної реакції на певну органічну сполуку; спочатку перегляньте відео. а потім виконуйте завдання. Робота не важка, проте потребує уваги та зосередженості. Тести виконуйте відповідно до відео, є запитання з кількома правильними відповідями.
Бажаю успіхів!
===============================================
Дата: 28/03 ( 9А, 9Б)
Тема: Взаємозв’язок між оксигеновмісними органічними сполуками.
Цілі уроку:
- закріпити знання про будову та властивості метанолу, етанолу, гліцерину, карбонових кислот , жирів та вуглеводів;
- повторити якісні реакції на етанол. гліцерин, етанову кислоту, глюкозу та крохмаль;
- виявити взаємозвязки між класами оксигеновмісних неорганічних сполук.
1) Повторіть матеріал підручника §26- §32.
2) Пригадайте молекулярні та структурні формули
- спиртів метанолу, етанолу, гліцерину;
- етанової, стеаринової, пальмітинової, олеїнової, ленолевої та леноленової кислот;
- жирів;
- вуглеводів глюкози, фруктози, сахарози, крохмалю та целюлози.
3) Перегляньте відеоурок
Взаємозв'язки між оксигеновсісними сполуками
4) Напишіть рівняння реакцій перетворення:
а) етен --> етанол --> етанова кислота --> пропилетаноат
б) вуглекислий газ --> глюкоза --> крохмаль --> глюкоза
в) олеїнова кислота --> стеаринова кислота --> тристеарат
5) Домашнє завдання :
Випишіть якісні реакції усіх оксигеновмісних речовин , які ми вивчили.
===============================================
Дата: 26/03 ( 9А, 9Б)
Тема: Крохмаль і целюлоза: полімерна будова, властивості, застосування. Л/д № 13,14. Реакція крохмалю з водою і розчином йоду.
Цілі уроку:
- ознайомитися з будовою та властивостями полісахаридів крохмаль та целюлоза;
- вивчити якісну реакцію на крохмаль;
- розширити свої знання про застосування полісахаридів.
1) Опрацюйте матеріал підручника §32, пригадайте визначення полімерів.
2) Перегляньте відеоурок з теми
Полісахариди: крохмаль та целюлоза
3) Особливу увагу зверніть на властивості та якісну реакцію на крохмаль
Л/д №13 Відношення крохмалю до води
Л/д №14 Якісна реакція на крохмаль
4) Порівняйте властивості моносахаридів та полісахаридів.
5) Виконайте перевірочну роботу ( за матеріалом §31 та §32) на платформі Мій Клас до 28 березня 21.00
===============================================
Дата: 19/03 ( 9А, 9Б)
Тема: Вуглеводи. Глюкоза і сахароза: будова, властивості, утворення в природі, застосування
Цілі уроку:
- ознайомитися з будовою, класифікацією та властивостями вуглеводів;
- вивчити хімічні властивості та добування глюкози та сахарози;
- розширити свої знання про застосування вуглеводів.
1) Опрацюйте матеріал підручника §31.
2) Перегляньте відеоурок з теми
3) Основні питання:
- класифікація вуглеводів( моносахариди, дисахариди, полісахариди);
- будова глюкози - альдегідоспирт;
- утворення в природу вуглеводів - процес фотосинтезу;
- якісні реакції на глюкозу з купрум(ІІ) гідроксидом;
- сахароза як дисахарид
4) Опрацюйте питання про значення глюкози для живих організмів (за матеріалами Інтернет)
5) Пригадайте задачі на визначення масової частки в розчинах та виконайте домашнє завдання:
Опрацюйте §31, письмово №231, №232
===============================================
Дата: 19/03 ( 9А, 9Б)
Тема: Жири. Склад жирів, їх утворення. Жири в природі, їх біологічна роль
Цілі уроку:
- ознайомитися з будовою, класифікацією та фізичними властивостями жирів;
- вивчити добуванням жирів та їх хімічні властивості;
- розширити свої знання про застосування жирів.
1) Опрацюйте матеріал підручника §30.
2) Перегляньте відеоурок з теми
3) Опрацюйте теоретичний матеріална платформі Мій Клас.
4) Виконайте перевірочну роботу на платформі Мій Клас до 21 березня 21.00
===============================================
Дата: 14/03 ( 9А, 9Б)
Тема: Поняття про вищі карбонові кислоти. Мило , його склад та мийна дія.
Цілі уроку:
- ознайомитися з будовою, класифікацією вищих карбоновиї кислот ;
- розглянути склад та властивості мила, його добування;
1) Опрацюйте матеріал підручника §29 , зверніть увагу :
- вищими називають органічні сполуки, що містять більше 10 атомів Карбону;
- вищі кислоти поділяються на насичені (стеаринова та пальмітинова) та ненасичені (олеїнова , ленолева та леноленова)
- мила - це натрієві ( тверді) та калієві (рідкі) солі вищих карбонових кислот.
2) Перегляньте відеоурок для закріплення прочитаного
3) Подумайте над питаннями :
- Які фізичні процеси лежать в основі миючої дії мила?
- Чому милом не можна прати у морській воді?
- Чи можна в домашніх умовах виготовити мило?
4) Домашнє завдання.
Вивчити §29 , письмово виконати №218
===============================================
Дата: 12/03, ( 9А, 9Б)
Тема: Практична робота № 4.
Властивості оцтової кислоти. Інструктаж з БЖД
Цілі уроку:
- експериментально дослідити хімічні властивостей етанової кислоти ;
- порівняти властивості етанової кислоти з неорганічними кислотами;
- повторити правила техніки безпеки при виконанні хімічних експериментів.
1) Повторіть матеріал підручника §28 .
2) перегляньте відеоурок практичної роботи, ніяких записів не виконуйте. зверніть увагу на хімічні досліди, а саме - ознаки та продукти реакцій
3) Виконайте завдання практичної роботи на платформі Мій Клас
===============================================
Дата: 05/03, 07/03 ( 9А, 9Б)
Тема: Етанова (оцтова) кислота. Функціональна карбоксильна група. Використання оцтової кислоти. Хімічні властивості етанової кислоти.
Цілі уроку:
- вивчити будову етанової кислоти як представника карбонових кислот , її характеристичну групу ;
- розглянути особливості фізичних властивостей етанової кислоти та її застосування;
- вивчити хімічні властивості етанової кислоти у порівнянні з неорганічними кислотами.
1) Опрацюйте матеріал підручника §28 , зверніть увагу на нову характеристичну групу
(Характеристична (функціональна ) група - це група атомів, що спричиняє певні фізичні та хімічні властивості речовини)
- СООН карбоксильна група, яка міститься в усіх карбонових кислотах і визначає більшість їх властивостей.
2) Перегляньте відеоурок для закріплення прочитаного
Будова, фізичні властивості та застосування етанової кислоти
3) Опрацюйте відеоурок , особливо рівняння реакцій в молекулярному та йонному видах
Хімічні властивості етанової(оцтової) кислоти
4) Запам'ятайте, що карбонові кислоти подібні до неорганічних , бо однаково реагують з :
- активними металами (до Н);
- основними та амфотерними оксидами;
- основами;
- солями слабших кислот (карбонатами. сульфідами, силікатами)
Відрізняються реакцією естерифікації - взаємодія карбонової кислоти та спитру з утворенням естеру та води
4) Домашнє завдання за 05/03
Виконайте письмово №209, №210(а)
5) Домашнє завдання за 07/03
Повторити теоретичний матеріал та виконати тестову роботу на платформі Мій Клас
до 11 березня 21.00
===============================================
Дата: 27/02 ( 9А, 9Б)
Тема: Метанол, етанол. Фізичні властивості та застосування спиртів. Фізіологічний вплив спиртів на організм людини.
Цілі уроку:
- повторити будову та хімічні властивості метанолу, етанолу, гліцеролу, поняття характеристичної групи , атомність спирту;
- розглянути фізичні властивості означених спиртів та їхні якісні реакції;
- ознайомитися із застосуванням та фізіологічним впливом на організм людини спиртів.
1) Опрацюйте матеріал підручника §27 , повторіть §26
2) Перегляньте відеоурок, перевірте себе на знання матеріалу попереднього уроку за тестами у цьому ролику
Значення спиртів та їх дія на організм людини
3) Для визначення спиртів використовують якісні реакції (запам'ятайте ознаки цих реакцій):
а) Якісна реакція на одноатомні спирти
4) Повторіть конспект попереднього уроку за 27 лютого
5) Домашнє завдання
Виконайте перевірочну роботу на платформі Мій Клас до 4 березня 21.00
===============================================
Дата: 27/02 ( 9А, 9Б)
Тема: Метанол, етанол, гліцерол. Хімічні властивості спиртів.
Цілі уроку:
- вивчити будову насичених спиртів, поняття характеристична група , атомність спирту;
- розглянути особливості фізичних властивостей спиртів;
- вивчти хімічні властивості спиртів на прикладі етанолу та гліцеролу.
1) Опрацюйте матеріал підручника §26 , зверніть увагу на нові поняття:
- Характеристична (функціональна ) група - це група атомів, що спричиняє певні фізичні та хімічні властивості речовини
- Атомність спирту - число груп ОН у складі спирту
2) Опрацюйте теоретичний матеріал за посиланням на платформі Мій Клас (хімічні властивості, рівняння реакцій)
3) Перегляньте відеоурок
4) Домашнє завдання
Прочитати §26
Допишіть рівняння рекцій
a) СН3ОН + Na -->
b) CH3OH + O2 -->
c) C3H5(OH)3+ Li -->
===============================================
Дата: 20/02 ( 9А, 9Б)
Тема: Вуглеводнева сировина й охорона довкілля. Застосування вуглеводнів.
Цілі уроку:
- повторити природні джерела вуглеводнів та їх застосування;
- отримати уявлення про вплив вуглеводнів та їх похідних на довкілля;
- ознайомитися із альтернативними джерелами енергії та їх застосуванням в умовах України.
1) Повторити матеріал підручника §24 .
2) Переглянути відеоурок
вплив використання вуглеводнів на довкілля та альтернатина енергія
3) Зверніть увагу на роль використання вуглецевоводневої сировини на атмосферу та гідросферу нашої планети.
4) Домашнє завдання
Сладіть повідомлення у робочому зошиті про одне з альтернативних джерел енергії
1) Енергія вітру
2) Енергія Сонця
3) Енергія припливів
4) Енергія води
5) Енергія біомаси
6) Геотермальна енергія
===============================================
Дата: 15/02 ( 9А, 9Б)
Тема: Перегонка нафти. Нафтопродукти.
Цілі уроку:
- вивчити принцип первинної та вторинної переробки нафти;
- ознайомитися з продуктами нафтопереробки та їх застосуванням
1) Повторіть матеріал підручника §24 та конспект попереднього уроку, на якому ми частково розглядати тему цього уроку.
2) Опрацюйте питання №1 та №2 у перевірочній роботі на платформі Мій клас, особливу увагу зверніть на процес крекінгу
3) Перегляньте відеурок
4) Виконайте перевірочну роботу на платформі Мій Клас до 19 лютого 21.00
(Розрахункова задача у роботі за темою §25 - закон об'ємних відношень)
===============================================
Дата: 13/02 ( 9А, 9Б)
Тема: Поширення вуглеводнів у природі . Природний газ, нафта, кам’яне вугілля – природні джерела вуглеводнів.
Цілі уроку:
- вивчити природні джерела вуглеводнів і деякі їхні властивості;
- отримати уявлення про склад нафти, природного і супутнього нафтового газів, вугілля;
- поповнити свої знання про застосування вуглеводнів.
1) Опрацюйте матеріал підручника §24 .
2) Перегляньте відеурок
3) Усно дайте відповідь на питання :
- Які вуглеводні містяяться у нафті?
- Чим відрізняється склад природного газу від супутного нафтового газу?
- Які речовини містяться у кам'яному вугіллі?
- В чому полягає видобування сланцевого газу?
4) Домашнє завдання :
Прочитайте §24 , письмово виконайте №188
===============================================
Дата: 08/02 ( 9А, 9Б)
Тема: Співвідношення об’ємів газів у хімічних реакціях. Обчислення об’ємних співвідношень газів за хімічними рівняннями.
Цілі уроку:
- вивчити закон об'ємних відношень;
- навчитися використовувати закон об'ємних відношень при обчисленнях об’ємних співвідношень газів за хімічними рівняннями.
1) Опрацюйте матеріал підручника §25 , зверніть особливу увагу на приклади розв'язування задач з цієї теми.
2) Закон об'ємних відношень: ОБ'ЄМИ ГАЗІВ У РЕАКЦІЯХ ВІДНОСЯТЬСЯ ОДИН ДО ОДНОГО, ЯК НЕВЕЛИКІ ЧИСЛА, ЩО ВІДПОВІДАЮТЬ КОЕФІЦІЄНТАМ У РІВНЯННЯХ РЕАКЦІЙ
Памятайте, що закон обємних відношень можна використовувати при розрахунках лише об'ємів газів!
3) Перегляньте відеурок
Розв'язування задач за законом об'ємних співвідношень
4) Повторіть властивості ненасичених вуглеводнів етилену та ацетилену
Властивості алкенів та алкінів
5) Виконайте перевірочну роботу на платформі Мій Клас до 14 лютого 21.00
===============================================
Дата: 06/02 ( 9А, 9Б)
Тема: Поліетилен.
Цілі уроку:
- вивчити будову , властивості та добування поліетилену;
- розглянути особливості реакцій полімеризації на прикладі етилену та ненасичених речовин;
- ознайомитися зі значенням полімерів та їхнім впливом на довкілля.
1) Опрацюйте матеріал підручника §23 , зверніть особливу увагу на принцип написання реакції полімеризації.
2) Перегляньте відеурок
Поліетилен та полімерні речовини
3) Запам'ятайте нові поняття:
- Полімеризація - реакція сполучення ненасичених речовин з утворення однієї високомолекулярної сполуки
- Полімер - високомолекулярна сполука (ВМС)
- Мономер - нтзькомолекулярна сполука, що утворює полімер у реакції полімеризації
- Структурна ланка - група атомів , що повторюється у складі полімерів
- Ступінь полімеризації - число структурних ланок
4) Перегляньте відео про вплив поліетилену на довкілля
Поліетиленовий пакет і довкілля
5) Виконайте письмово за матеріалами Інтернет №181
===============================================
Дата: 01/02 ( 9А, 9Б)
Тема: Етилен та ацетилен: молекулярні, електронні, структурні формули, фізичні властивості. Хімічні властивості ненасичених вуглеводнів, їх застосування.
Цілі уроку:
- вивчити будову ненасичених вуглеводнів - алкенів та алкінів на прикладі етилену та ацетилену;
- розглянути особливості реакцій приєднання та горіння етилену та ацетилену;
- навчитися записувати хімічні рівняння у молекулярній та скороченій структурній формі
1) Опрацюйте матеріал підручника §21 , пригадайте , що таке реакції сполучення
2) Опрацюйте теоретичний матеріал за посиланням
Будова ненасичених вуглеводнів
3) Перегляньте відеоурок про властивості ненасичених вуглеводнів
===============================================
Дата: 30/01 ( 9А, 9Б)
Тема: Розв'язування вправ та розрахункових задач
Цілі уроку:
- повторити хімічні властивості алканів;
- розглянути особливості реакцій заміщення з галогенами та горіння;
- навчитися визначати молекулярну формулу вуглеводнфі за молекулярною масою та відносною густиною.
1) Повторіть матеріал підручника на ст.126-129 , пригадайте, що таке реакції заміщення та горівння в неорганічній хімії
2) Пригадайте особливості хімічних реакцій метану за посиланням
==================================================
Дата: 25/01 ( 9А, 9Б)
Тема: Хімічні властивості алканів.
Цілі уроку:
- вивчити хімічні властивості насичених вуглеводнів - алканів;
- розглянути особливості реакцій заміщення з галогенами та горіння;
- навчитися записувати хімічні рівняння з органічними речовинами у молекулярній формі.
1) Опрацюйте матеріал підручника на ст.126-129 , пригадайте . що таке реакції заміщення та горівння в неорганічній хімії
2) Опрацюйте теоретичний матеріал за посиланням
==================================================
Дата: 23/01 ( 9А, 9Б)
Тема: Ізомерія насичених вуглеводнів.
Цілі уроку:
- вивчити поняття ізомерії на прикладі насичених вуглеводнів;
- розглянути особливості структурної ізомерії алканів;
- навчитися давати назви ізомерам алканів за систематичною номенклатурою
1) Опрацюйте матеріал підручника на ст.121-122 та перегляньте конспекти попередніх двох уроків, зверніть увагу на структурні формули та спрощені структурні формули алканів.
2) Перегляньте відеоурок
4) Домашнє завдання: Виконайте 1) №31 з скріна
2) Напишіть структурні формули алканів за їх назвами
а) 2,3-диметилгексан;
б) 3-етил-4-пропилгептан;
в) 2,2,3,5-тетраметил-5-пропилоктан
Дата: 18/01 ( 9А, 9Б)
Тема: Гомологи метану. Молекулярні та структурні формули, фізичні властивості гомологів метану.
Цілі уроку:
- вивчити склад насичених вуглеводнів, їх загальну формулу;
- розглянути особливості просторової будови алканів та їхні фізичні властивості ;
- закріпити уміння складати скорочені стуктурні формули алканів нормальної та розгалудженої будови.
1) Опрацюйте §20 та конспект попереднього уроку, зверніть увагу на поняття гомологів
2) Розгляньте таблицю 2 на ст.118, повторіть нумерологію ( урок 11/01)
3) Перегляньте відеоурок
Дата. 16/01 ( 9А, 9Б)
Тема: Метан як представник насичених вуглеводнів: молекулярна, електронна, структурна формули, поширення в природі.
Цілі уроку:
- вивчити , що таке вуглеводні;
- розглянути особливості просторової будови молекули метану та його фізичні властивості ;
- закріпити уміння складати скорочені стуктурні формули органічних сполук з урахуванням валентностей атомів.
1) Опрацюйте §19 та конспект уроку, зверніть увагу на електронно-графічну формулу атому Карбону та просторову будову метану.
2) Перегляньте відеоурок та опрацюйте матеріал про будову атомів Карбону в насичених вуглеводнях
Дата. 11/01 ( 9А, 9Б)
Тема: Особливості ковалентного зв'язку в органічних сполуках. Структурні формули.
Цілі уроку:
- прослідити взаємозалежність складу, будови та властивостей органічних сполук;
- вивчити особливості ковалентного зв'язку між атомами Карбону;
- закріпити уміння складати стуктурні формули органічних сполук з урахуванням валентностей атомів.
1) Повторіть §18 та конспект попереднього уроку, зверніть увагу на особливості органічних сполук.
2) Перегляньте відеоурок та опрацюйте матеріал про особливості ковалентних звя'зків між атомами Карбону ( одинарні, подвійні, потрійні, сігма- та пі-зв'язки )
=========================================================================
Дата : 09/01 (9А, 9Б)
Тема: Загальні і відмінні ознаки органічних і неорганічних сполук.
( Урок в Zoom)
Цілі уроку:
- з’ясувати відмінності органічних речовин від неорганічних;
- зрозуміти причини великої численності органічних сполук, повторити структурні формули;
- дізнатися про практичне значення досягнень угалузі органічної хімії.
1) Прочитайте §18, зверніть увагу на особливості органічних сполук.
2) Перегляньте відеоурок , закріпіть прочитане у підручнику
4) ВИКОНАЙТЕ ПЕРЕВІРОЧНУ РОБОТУ НА ПЛАТФОРМІ МІЙ КЛАС ДО 11 СІЧНЯ 21.00
(Рекомендації щодо виконання роботи у самій роботі)
=========================================================================
Дата : 9А, 9Б - 19/12
Урок 29. Швидкість хімічної реакції.
Цілі уроку:
- повторити поняття про хімічної реакції, реагенти та продукти реакції, умови перебігу хімічної реакції;
- вивчити плив різних чинників на швидкість перебігу хімічної реакції;
- навчитися прогнозувати зміну швидкості хімічної реакції від зміни умов її перебігу.
1) Опрацюйте пар.17
2) Зверніть увагу на чинники , що впливають на швидкість реакції
- хімічна природа реагуючих речовин ( активність речовин);
• концентрації реагентів (якщо взаємодіють гази або розчинені речовини);
• площа поверхні контакту речовин (у неоднорідних сумішах);
• температура;
• наявність сторонніх речовин (каталізаторів)
3) Перегляньте відеоурок з експериментальною частиною
4) Виконайте роботу на платформі Мій Клас до 21 грудня 19.00
======================================================================
Дата : 9А, 9Б - 14/12
Урок 28. Тепловий ефект реакції. Екзо і ендотермічні реакції. Термохімічні рівняння .
Цілі уроку:
- повторити поняття про оборотні та необоротні реакції;
- закріпити знання про енергентичний аспект утворення та руйнування хімічного зв'язку;
- вивчити поняття тепловий ефект, термохімічне рівняння та навчитися складати та розрізняти рівняння екзотермічних та ендотермічних реакцій.
1) Прочитайте матеріал підручника на ст.76-77, перегляньте короткий відеоурок та згадайте , що таке оборотні та необоротні реакції ( при вивченні реакцій йонного обміну)
2) Прочитайте §16, випишіть у робочий зошит визначення:
- тепловий ефект реакції
- ендотермічна реакція;
- екзотермічна реакція;
- термохімічне рівняння.
3) Перегляньте відеоурок для закріплення прочитаного



Немає коментарів:
Дописати коментар